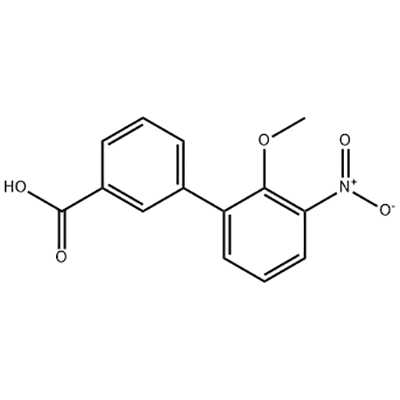
2'-メトキシ-3'-ニトロ-ビフェニル-3-カルボン酸
2'-メトキシ-3'-ニトロ-ビフェニル-3-カルボン酸
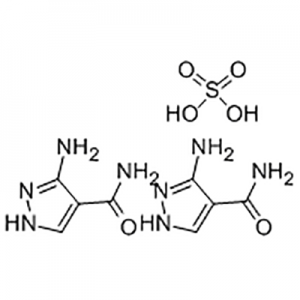
2'-メトキシ-3'-ニトロ-ビフェニル-3-カルボン酸は、エルトロンボパグの中間体として使用されます。
英国のグラクソ・スミスクライン (GSK) によって開発され、その後スイスのノバルティスと共同開発されたエルトロンボパグは、世界で最初で唯一承認された小分子非ペプチド TPO 受容体アゴニストです。エルトロンボパグは、2008 年に特発性血小板減少性紫斑病 (ITP) の治療薬として、2014 年に重度の再生不良性貧血 (AA) の治療薬として米国 FDA によって承認されました。また、この 30 年間で AA の治療薬として米国 FDA によって承認された最初の薬でもあります。
2012年12月、米国FDAは慢性C型肝炎(CHC)患者の血小板減少症の治療薬としてエルトロンボパグを承認し、血小板数が少ないため予後不良のC型肝炎患者がインターフェロンベースの肝臓疾患の標準治療を開始し、維持できるようにした。2014年2月3日、グラクソ・スミスクラインは、免疫療法に完全に反応しなかった重度のケミカルブック再生不良性貧血(SAA)患者の血球減少症の治療に対するエルトロンボパグの画期的な治療薬認定をFDAが認めたと発表した。2015年8月24日、米国FDAは、コルチコステロイド、免疫グロブリン、脾臓摘出術に対する反応が不十分な慢性免疫性血小板減少症(ITP)の成人および1歳以上の小児の血小板減少症の治療薬としてエルトロンボパグを承認しました。2018 年 1 月 4 日、エルトロンボパグは中国で原発性免疫性血小板減少症 (ITP) の治療薬として承認されました。
ここにメッセージを書いて送信してください



![ペンタメチレン ビス[1-(3,4-ジメトキシベンジル)-3,4-ジヒドロ-6,7-ジメトキシ-1H-イソキノリン-2-プロピオネート]、ジオキサレート](http://cdn.globalso.com/jindunchem-med/image281-300x300.png)

![カスプウンギン酢酸塩;カスポファンギン酢酸塩;カンシダス;カスポファンギン酢酸塩 [米国:BAN:JAN];](http://cdn.globalso.com/jindunchem-med/fbe17385-300x300.jpg)